Covid-19, La strategia europea sui vaccini. «Lo sviluppo del vaccino è un processo complesso e lungo che richiede circa 10 anni».
(AGENPARL) – Roma, 29 luglio 2021 – Interessante, molto interessante è la lettura della strategia europea sui vaccini.
Da legge anche se è lungo, ma vale la pena. Buona lettura.
Lo sviluppo e la distribuzione di vaccini sicuri ed efficaci contro il COVID-19 rappresenta una risposta duratura alla pandemia. È al centro della risposta della Commissione europea al coronavirus, si legge sul sito della Commissione europea.
Come è noto la Commissione e gli Stati membri hanno adottato un approccio comune dell’UE per garantire le forniture e facilitare l’introduzione dei vaccini.
Inoltre, la Commissione ha stipulato accordi di acquisto anticipato con i singoli produttori di vaccini per conto degli Stati membri. In cambio del diritto di acquistare un determinato numero di dosi di vaccino in un determinato periodo di tempo e ad un determinato prezzo, la Commissione ha finanziato una parte dei costi iniziali sostenuti dai produttori di vaccini tramite lo strumento di sostegno alle emergenze da 2,7 miliardi di euro .
Questo finanziamento è considerato un acconto sui vaccini che gli Stati membri acquistano. Un ulteriore sostegno ai produttori di vaccini è possibile tramite prestiti della Banca europea per gli investimenti. Questo approccio ridurrà i rischi per le aziende accelerando la produzione.
Un ampio portafoglio di vaccini basato su diversi approcci tecnologici massimizza le possibilità di sviluppo e distribuzione di vaccini sicuri ed efficaci. Con questo in mente, il 17 giugno 2020, la Commissione europea ha presentato la strategia dell’UE sui vaccini per accelerare lo sviluppo, la produzione e la diffusione di vaccini contro il COVID-19.
La Commissione ha deciso di sostenere vari vaccini sulla base di una solida valutazione scientifica, della tecnologia utilizzata e della capacità di rifornire l’intera UE.
Lo sviluppo del vaccino è un processo complesso e lungo, che normalmente richiede circa 10 anni. Con la strategia sui vaccini, la Commissione ha sostenuto gli sforzi e ha reso lo sviluppo più efficiente, con la conseguente distribuzione di vaccini sicuri ed efficaci nell’UE entro la fine del 2020. Questo risultato ha richiesto l’esecuzione di sperimentazioni cliniche in parallelo con investimenti nella capacità di produzione per poter produrre milioni di dosi di un vaccino di successo. Le procedure di autorizzazione e gli standard di sicurezza rigorosi e robusti sono sempre rispettati.
Ad oggi, 4 vaccini sicuri ed efficaci contro COVID-19 sono stati autorizzati per l’uso nell’UE a seguito di raccomandazioni scientifiche positive dell’Agenzia europea per i medicinali:
BioNTech-Pfizer
Il 21 dicembre 2020, la Commissione europea ha concesso un’autorizzazione all’immissione in commercio condizionata per il vaccino COVID-19 sviluppato da BioNTech e Pfizer, rendendolo il primo vaccino COVID-19 autorizzato nell’UE.
Ciò fa seguito a una raccomandazione scientifica positiva basata su una valutazione approfondita della sicurezza, dell’efficacia e della qualità del vaccino da parte dell’Agenzia europea per i medicinali ed è approvata dagli Stati membri.
L’accordo di acquisto anticipato con BioNTech-Pfizer prevede l’acquisto iniziale di 200 milioni di dosi per conto di tutti gli Stati membri dell’UE, più un’opzione per l’acquisto fino a ulteriori 100 milioni di dosi. Il 15 dicembre 2020 la Commissione ha deciso di acquistare questi 100 milioni di dosi aggiuntive.
Inoltre, l’8 gennaio 2021, la Commissione ha proposto agli Stati membri di acquistare ulteriori 200 milioni di dosi di vaccino BioNTech-Pfizer, con la possibilità di acquisire altri 100 milioni di dosi.
Gli Stati membri possono decidere di donare il vaccino ai paesi a basso e medio reddito o di reindirizzarlo ad altri paesi europei.
Il 10 marzo 2021, la Commissione europea ha raggiunto un accordo con BioNTech-Pfizer per la fornitura di 4 milioni di dosi in più di vaccini COVID-19 agli Stati membri per affrontare gli hotspot del coronavirus e facilitare la libera circolazione transfrontaliera. Queste dosi si aggiungono al programma di consegne attualmente concordato tra gli Stati membri e BioNTech-Pfizer.
Il 20 maggio 2021, la Commissione Europea ha firmato un terzo contratto con BioNTech-Pfizer. Riserva 1,8 miliardi di dosi aggiuntive per conto di tutti gli Stati membri dell’UE, tra la fine del 2021 e il 2023. Permetterà l’acquisto di 900 milioni di dosi dell’attuale vaccino e di un vaccino adattato alle varianti (se necessario e se approvato), con la possibilità di acquistare ulteriori 900 milioni di dosi.
Con l’accordo di BioNTech-Pfizer, è disponibile il contratto di acquisto anticipato redatto . Disponibile anche il contratto di compravendita.
Moderna
Il 6 gennaio 2021, la Commissione europea ha concesso un’autorizzazione all’immissione in commercio condizionata per il vaccino contro il COVID-19 sviluppato da Moderna, rendendolo il secondo vaccino autorizzato per l’uso nell’UE.
Ciò fa seguito a una raccomandazione scientifica positiva basata su una valutazione approfondita della sicurezza, dell’efficacia e della qualità del vaccino da parte dell’Agenzia europea per i medicinali ed è approvata dagli Stati membri.
L’accordo di acquisto anticipato con Moderna prevede l’acquisto iniziale di 80 milioni di dosi per conto di tutti gli Stati membri dell’UE, più la possibilità di richiedere fino a ulteriori 80 milioni di dosi. Il 15 dicembre 2020 la Commissione ha deciso di acquistare 80 milioni di dosi aggiuntive.
Il 17 febbraio 2021 la Commissione Europea ha approvato un secondo contratto con l’azienda farmaceutica Moderna, che prevede un ulteriore acquisto di 300 milioni di dosi (150 milioni nel 2021 e un’opzione per l’acquisto di ulteriori 150 milioni nel 2022) per conto di tutta l’UE Stati membri.
Il 22 giugno 2021 la Commissione ha approvato una modifica al secondo contratto per l’attivazione dei 150 milioni di dosi facoltative nel 2022.
Con l’accordo di Moderna sono disponibili il Contratto di Acquisto Anticipato redatto e il Contratto di Compravendita redatto .
AstraZeneca
Il 29 gennaio 2021, la Commissione europea ha concesso un’autorizzazione all’immissione in commercio condizionata per il vaccino contro il COVID-19 sviluppato da AstraZeneca, rendendolo il terzo vaccino autorizzato per l’uso nell’UE.
Questa autorizzazione segue una raccomandazione scientifica positiva basata su una valutazione approfondita della sicurezza, dell’efficacia e della qualità del vaccino da parte dell’Agenzia europea per i medicinali ed è approvata dagli Stati membri.
Con l’accordo di AstraZeneca, la Commissione ha reso pubblico il contratto di acquisto anticipato redatto .
Il 18 giugno 2021, il Tribunale di primo grado di Bruxelles ha ordinato ad AstraZeneca di fornire dosi di vaccino all’UE.
Johnson & Johnson
L’11 marzo 2021, la Commissione europea ha rilasciato un’autorizzazione all’immissione in commercio condizionata per il vaccino COVID-19 sviluppato da Janssen Pharmaceutica NV, una delle società farmaceutiche Janssen di Johnson & Johnson, rendendolo il quarto vaccino autorizzato per l’uso nell’UE. Questa autorizzazione segue una raccomandazione scientifica positiva basata su una valutazione approfondita della sicurezza, dell’efficacia e della qualità del vaccino da parte dell’Agenzia europea per i medicinali ed è approvata dagli Stati membri. Con l’autorizzazione al mercato condizionata, Janssen sarà in grado di consegnare all’UE 200 milioni del suo vaccino monodose COVID-19 a partire dal secondo trimestre del 2021. Il contratto, che è stato chiuso il 7 ottobre 2020, consente agli Stati membri di acquistare un ulteriori 200 milioni di dosi.
Con l’accordo di Johnson & Johnson, la Commissione ha reso pubblico il contratto di acquisto anticipato redatto.
Vaccini ancora in fase di sviluppo
Sono stati stipulati 2 contratti che consentono l’acquisto di un vaccino una volta dimostratosi sicuro ed efficace:
Sanofi-GSK
Il 18 settembre 2020 è entrato in vigore l’ accordo di acquisto anticipato negoziato per conto degli Stati membri dell’UE tra Sanofi-GSK e la Commissione europea .
Una volta che il vaccino si è dimostrato sicuro ed efficace, il contratto consente a tutti gli Stati membri dell’UE di acquistare fino a 300 milioni di dosi del vaccino.
Fatte salve le considerazioni normative, le aziende mirano a rendere disponibile il vaccino entro la seconda metà del 2021. Sanofi e GSK si adopereranno anche per fornire una parte significativa della loro fornitura di vaccini attraverso una collaborazione con la struttura COVID-19 Vaccines Global Access (COVAX) – il pilastro vaccinale dell’Acceleratore di strumenti per l’accesso al COVID-19 per i paesi a reddito medio e basso.
Con l’accordo di Sanofi-GSK, è disponibile il contratto di acquisto anticipato redatto.
CureVac
Il 19 novembre 2020 è entrato in vigore il contratto negoziato per conto degli Stati membri dell’UE tra CureVac e la Commissione.
Una volta che il vaccino si sarà dimostrato sicuro ed efficace, il contratto prevede l’acquisto iniziale di 225 milioni di dosi per conto di tutti gli Stati membri dell’UE, oltre alla possibilità di richiedere fino a ulteriori 180 milioni di dosi.
CureVac, una società europea con sede in Germania, ha firmato il 6 luglio 2020 un contratto di prestito di 75 milioni di euro con la Banca europea per gli investimenti per lo sviluppo e la produzione su larga scala di vaccini.
Con l’accordo di CureVac, la Commissione ha reso pubblico il contratto di acquisto anticipato redatto.
Colloqui esplorativi
I colloqui esplorativi dovrebbero sfociare in un accordo di acquisto anticipato da finanziare attraverso lo strumento di supporto alle emergenze , che dispone di fondi dedicati alla creazione di un portafoglio di potenziali vaccini prodotti da diverse aziende.
Le aziende con un candidato vaccino promettente, già in fase di avvio o in procinto di iniziare le sperimentazioni cliniche, sono invitate a contattare la Commissione all’indirizzo EC-VACCINES@ec.europa.eu
Novavax
Il 17 dicembre 2020, la Commissione ha concluso colloqui esplorativi con l’azienda farmaceutica Novavax, in vista dell’acquisto del suo potenziale vaccino contro il COVID-19.
Il vaccino Novavax è un prodotto a subunità proteica già in fase di sperimentazione clinica di fase 3. Il contratto previsto prevederebbe la possibilità per tutti gli Stati membri dell’UE di acquistare inizialmente 100 milioni di dosi, seguite da 100 milioni di dosi aggiuntive.
Valneva
Il 12 gennaio 2021, la Commissione ha concluso colloqui esplorativi con l’azienda farmaceutica Valneva in vista dell’acquisto del suo potenziale vaccino contro il COVID-19.
Il contratto previsto con Valneva prevederebbe la possibilità per tutti gli Stati membri dell’UE di acquistare 30 milioni di dosi e potrebbero acquistare fino a 30 milioni di dosi in più.
Gli obiettivi della strategia europea sui vaccini sono:
garantire la qualità, la sicurezza e l’efficacia dei vaccini;
garantire l’accesso tempestivo ai vaccini per gli Stati membri e la loro popolazione guidando al contempo lo sforzo di solidarietà globale;
garantire un accesso equo e conveniente per tutti nell’UE a un vaccino a prezzi accessibili il prima possibile;
assicurandosi che nei paesi dell’UE vengano fatti i preparativi per quanto riguarda l’introduzione di vaccini sicuri ed efficaci, affrontando le esigenze di trasporto e distribuzione e identificando i gruppi prioritari che dovrebbero avere accesso ai vaccini prima.
La strategia sui vaccini dovrebbe fungere da punto di riferimento per gli Stati membri nella formulazione delle loro strategie nazionali.
Due pilastri
Garantire la produzione di una quantità sufficiente di vaccini nell’UE attraverso accordi di acquisto anticipato con i produttori di vaccini tramite lo strumento di sostegno alle emergenze. Oltre a tali accordi possono essere resi disponibili ulteriori finanziamenti e altre forme di sostegno.
Adattare le norme dell’UE all’attuale urgenza al fine di accelerare lo sviluppo, l’autorizzazione e la disponibilità dei vaccini mantenendo gli standard di qualità, sicurezza ed efficacia dei vaccini.
Preparazione alla vaccinazione nei paesi dell’UE
La vaccinazione salva la vita. La vaccinazione su larga scala contro il COVID-19 è lo strumento chiave per controllare il virus.
Il 15 ottobre 2020, la Commissione europea ha pubblicato una comunicazione sulla preparazione alle strategie di vaccinazione contro il COVID-19 e alla diffusione del vaccino. Gli elementi chiave da considerare per le strategie nazionali di vaccinazione includono:
la capacità dei servizi di vaccinazione di fornire vaccini contro il COVID-19, compresa la forza lavoro qualificata e i dispositivi medici e di protezione;
facile accesso ai vaccini per le popolazioni target, sia per l’accessibilità economica che per la vicinanza fisica;
la diffusione di vaccini con caratteristiche ed esigenze di stoccaggio e trasporto diverse, in particolare in termini di catena del freddo, trasporto refrigerato e capacità di stoccaggio;
comunicazione chiara sui benefici, i rischi e l’importanza dei vaccini contro il COVID-19 per costruire la fiducia del pubblico.
Possibili gruppi di priorità
Con l’aumento della disponibilità di vaccini, le strategie nazionali dovranno essere adeguate di conseguenza. Ad esempio, all’inizio probabilmente ci si concentrerà sulla riduzione del tasso di decessi e dell’onere sui servizi essenziali. Più avanti nel processo di diffusione della vaccinazione, ciò potrebbe spostarsi verso la riduzione di più ampie restrizioni sociali ed economiche.
Si dovrebbero prendere in considerazione i seguenti gruppi di priorità (non classificati):
operatore sanitario
persone di età superiore ai 60 anni
persone il cui stato di salute li rende particolarmente a rischio
lavoratori essenziali al di fuori del settore sanitario
lavoratori che non possono allontanarsi socialmente
gruppi socioeconomici vulnerabili e altri gruppi a rischio più elevato
Velocizzare la vaccinazione nell’UE
Il 19 gennaio 2021, la Commissione europea ha adottato una comunicazione che invita gli Stati membri ad accelerare l’introduzione dei vaccini in tutta l’UE.
A metà luglio, l’Europa disponeva di dosi di vaccino sufficienti per vaccinare il 70% della popolazione adulta dell’UE.
I progressi della vaccinazione in Europa possono essere seguiti sul sito web del Centro europeo per la prevenzione e il controllo delle malattie ( ECDC ).
Aumentare la produzione di vaccini industriali nell’UE
Il 4 febbraio 2021, la Commissione europea ha istituito una task force sotto l’autorità del commissario per il mercato interno, Thierry Breton, in collaborazione con il commissario per la salute e la sicurezza alimentare, Stella Kyriakides.
La task force mira ad aumentare la capacità di produzione di vaccini nell’UE, fungendo da sportello unico per i produttori che necessitano di sostegno, e a identificare e affrontare le strozzature nella capacità di produzione e nelle catene di approvvigionamento.
I contatti regolari della task force con l’industria e gli Stati membri consentono alla Commissione di avere una buona conoscenza delle capacità di produzione di vaccini nell’UE. La task force aggiorna inoltre regolarmente una mappatura delle capacità di produzione di vaccini nell’UE, compresa la relativa catena di approvvigionamento dell’UE.
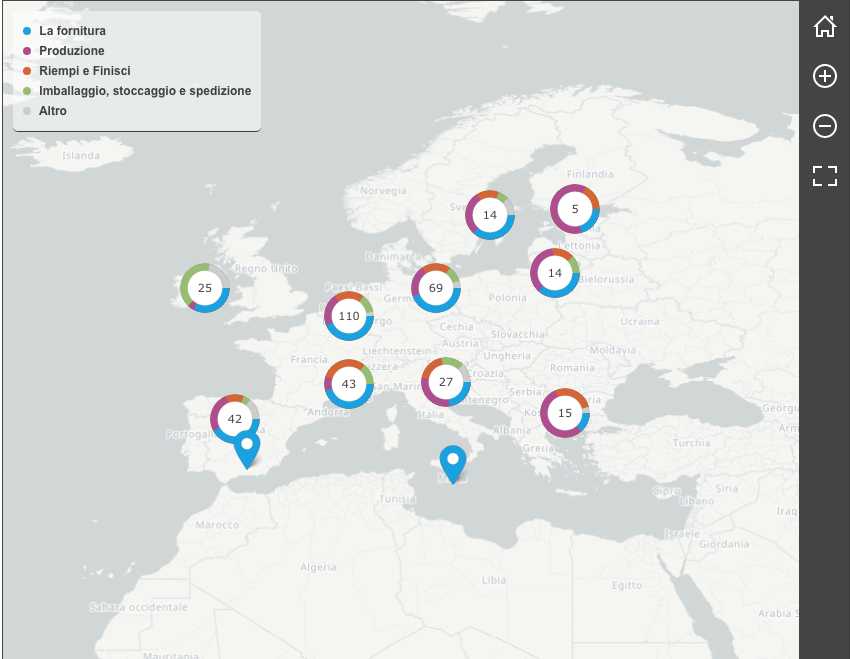
L’esercizio di mappatura si basa sui dati acquisiti attraverso le attività della task force, dall’evento di matchmaking organizzato dalla Commissione nel marzo 2021 con le aziende che hanno acconsentito alla pubblicazione del proprio nome, informazioni pubblicamente disponibili e informazioni condivise dagli Stati membri. Questi dati saranno integrati e aggiornati non appena saranno disponibili ulteriori informazioni.
La Task Force ha classificato le aziende in base alla loro principale area di attività, quindi le aziende possono avere più capacità che potrebbero non essere riflesse nella mappa. I dati nell’esercizio di mappatura sono aggregati in cinque categorie principali ai fini della visualizzazione come segue:
Approvvigionamento (produzione/fornitura materie prime, materiali di consumo, monouso, attrezzature)
Produzione (produzione e formulazione, CDMO/CMO)
Riempi & Finisci, Imballaggio
Stoccaggio e spedizione
Altro (sviluppo di processi di vaccini, CRO, R&D, servizi di gestione delle sperimentazioni cliniche)
Il 12 luglio 2021, la Task Force ha organizzato un secondo evento di matchmaking, questa volta sulle terapie COVID-19, per promuovere collaborazioni industriali per accelerare lo sviluppo e la produzione di farmaci nuovi o riproposti per il trattamento di COVID-19.
Certificato digitale UE COVID
Il 17 marzo 2021 la Commissione ha adottato una proposta legislativa che istituisce un quadro comune per un certificato digitale dell’UE contro la COVID che copre la vaccinazione, i test e il recupero. Si tratta di un approccio a livello dell’UE per il rilascio, la verifica e l’accettazione di certificati per facilitare la libera circolazione all’interno dell’UE, basato su un rigoroso rispetto della non discriminazione e dei diritti fondamentali dei cittadini dell’UE. Il 1° luglio 2021 è entrato in vigore il regolamento sul Certificato UE Digital COVID.
Cooperazione globale
Il 18 settembre 2020, la Commissione europea ha confermato la sua partecipazione allo strumento COVAX per un accesso equo a vaccini COVID-19 a prezzi accessibili. La prima previsione di distribuzione è disponibile .
COVAX è il pilastro dei vaccini dell’acceleratore Access to COVID-19 Tools (ACT), una collaborazione globale per accelerare lo sviluppo, la produzione e l’accesso equo a test, trattamenti e vaccini COVID-19.
Il 12 novembre 2020, l’Unione europea ha annunciato che contribuirà con ulteriori 100 milioni di euro in sovvenzioni per sostenere lo strumento COVAX per garantire l’accesso al futuro vaccino contro il COVID-19 nei paesi a basso e medio reddito.
I fondi integreranno i 400 milioni di euro di garanzie già impegnate dall’UE per COVAX, rendendo l’Unione uno dei principali donatori. Con questo nuovo contributo, l’UE intensifica ulteriormente gli investimenti a sostegno della ripresa globale con un totale di 500 milioni di euro.
ACT riunisce governi, scienziati, imprese, società civile, filantropi e organizzazioni sanitarie globali come
la Fondazione Bill & Melinda Gates
l’ OMS
Strumento di finanziamento globale
Nella sua comunicazione del 19 gennaio 2021, la Commissione ha annunciato che istituirà un meccanismo di condivisione dei vaccini dell’UE per strutturare la fornitura di vaccini condivisi dagli Stati membri con i paesi partner attraverso un approccio Team Europe, prestando particolare attenzione ai Balcani occidentali, e il vicinato meridionale e l’Africa.
La prima previsione di distribuzione è disponibile .
